VALIDACIÓN CLÍNICA: La Evidencia que Respalda el Modelo
El CDSS Tissunómico no es un ejercicio teórico aislado. Cada componente del algoritmo — desde la eficacia del T-DXd en diferentes niveles de expresión HER2 hasta el impacto de la heterogeneidad espacial en la respuesta terapéutica — está respaldado por evidencia clínica de ensayos fase III y estudios translacionales recientes. Esta sección presenta la validación clínica organizada por los pilares fundamentales del modelo.
PILAR 1: El T-DXd Funciona Across Todo el Espectro de Expresión HER2
El modelo asume que el T-DXd puede destruir células tumorales independientemente de si expresan niveles altos, bajos o mínimos de HER2, siempre que exista proximidad espacial a células que sí lo expresen. Esta premisa está validad por el programa de ensayos clínicos DESTINY-Breast:
- HER2-positivo (IHC 3+ o IHC 2+/ISH+): DESTINY-Breast01 (fase II, n=184)... ORR 62.0%, mediana de PFS 19.4 meses (análisis actualizado con seguimiento mediano de 26.5 meses; Saura et al., Ann Oncol 2024).[1] | DESTINY-Breast03 (fase III, n=524)... mediana de PFS 28.8 meses vs 6.8 meses (segundo análisis interino; Hurvitz et al., Lancet 2023), confirmada en el análisis a largo plazo con seguimiento de 41 meses: PFS 29.0 vs 7.2 meses, OS 52.6 vs 42.7 meses (Cortés et al., Nat Med 2024), ORR 79% vs 35%.[2]
- HER2-low (IHC 1+ o IHC 2+/ISH-): DESTINY-Breast04 (fase III, n=557)... PFS 9.9 vs 5.1 meses, OS 23.4 vs 16.8 meses.[3,4]
- HER2-ultralow (IHC 0 con tinción de membrana): DESTINY-Breast06 (fase III, n=866)... PFS 13.2 vs 8.1 meses. ORR 61.8% vs 26.3% en la población completa HER2-ultralow (Bardia et al., NEJM 2024).[5]
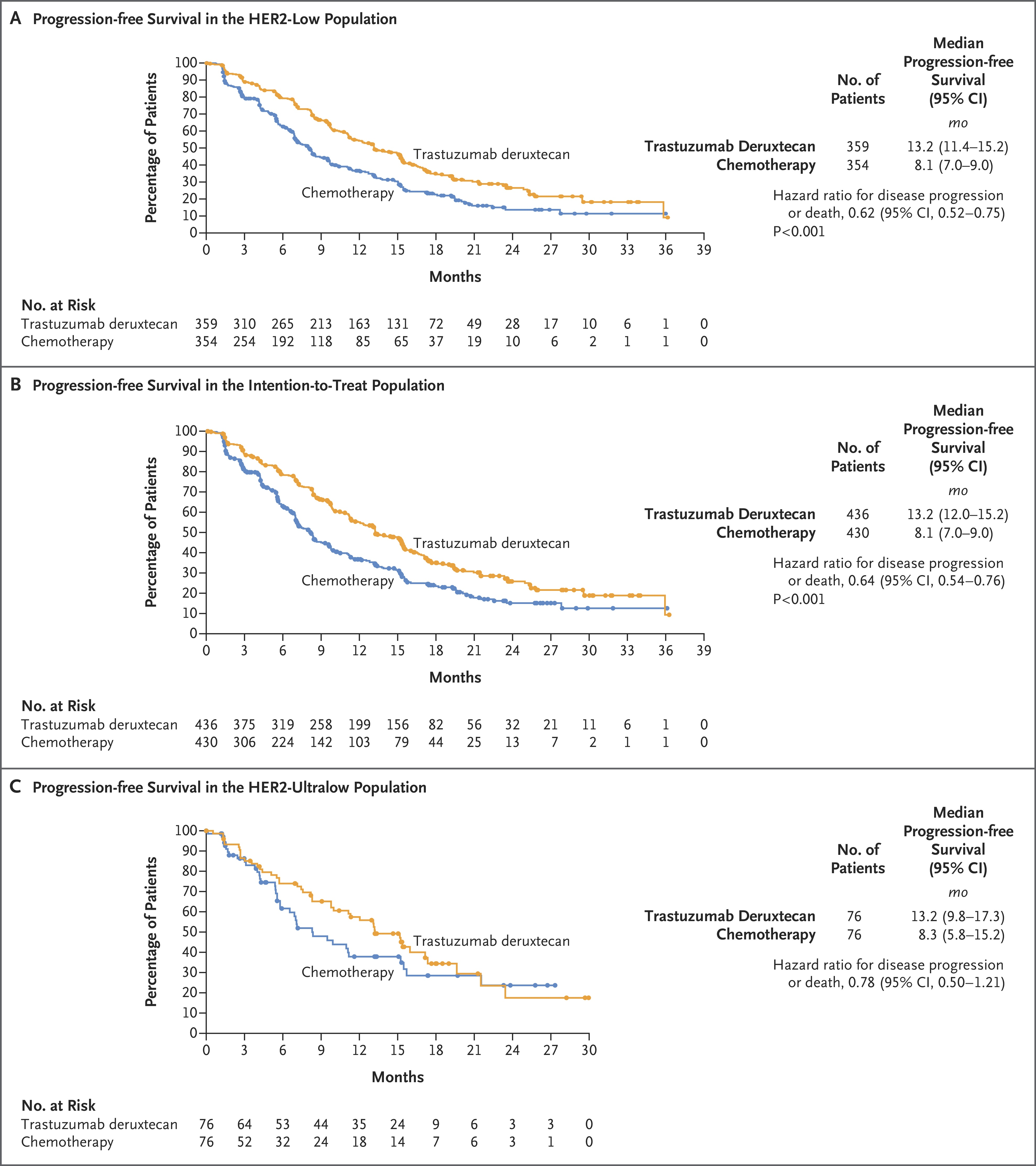
La FDA aprobó el T-DXd para tumores HER2-low (2022) y HER2-ultralow (2025)...[6,7]
PILAR 2: El Efecto Bystander Es el Mecanismo Clave en Tumores HER2-Heterogéneos
El modelo asume que la toxina DXd difunde desde las células HER2-positivas hacia las HER2-negativas vecinas.
- Visualización directa: Suzuki et al. (2021) utilizaron imágenes de Phosphor-Integrated Dots (PID) en modelos de xenoinjerto HER2-heterogéneos, demostrando que mientras el anticuerpo trastuzumab se localiza exclusivamente en áreas HER2-positivas, la toxina DXd difunde hacia las áreas HER2-negativas adyacentes, confirmando visualmente el efecto bystander in vivo.[8]
- Cuantificación de penetración: Khera et al. (2021, 2022) cuantificaron la penetración del payload bystander con resolución celular en esferoides 3D y tejido tumoral, demostrando que los payloads lipofílicos de ADCs penetran 2-5 capas celulares (30-80 μm) antes de perder concentración letal, y que esta distancia puede modelarse matemáticamente mediante funciones de decaimiento exponencial.[9,10]
- Mecanismo molecular: Tsao et al. (2025) demostraron que la eficacia del T-DXd en tumores HER2-low/negative puede ser independiente de la internalización del ADC, dependiendo en cambio de proteasas extracelulares como la catepsina L (CTSL) presentes en el estroma tumoral, que clivan el linker del T-DXd y liberan el DXd directamente en el microambiente. Este mecanismo no está modelado en el CDSS actual y constituye una limitación documentada.[11]
PILAR 3: La Heterogeneidad Intratumoral de HER2 Predice Resistencia
El modelo incorpora el índice HER2-HQE como métrica complementaria porque la heterogeneidad intratumoral predice resistencia:
- Evidencia clínica: Metzger Filho et al. (2021) pCR 0% vs 55%.[12] | Hu et al. (2026) pCR 24.5% vs 62.5%.[13] | Li et al. (2024) análisis transcriptómico.[14]
- Mecanismos: Goyette et al. (2026) demostraron cooperación subclonal HER2hi/HER2lo.[15]
PILAR 4: La Distribución Espacial Predice la Respuesta al T-DXd
- El cSPS: El continuous Spatial Proximity Score (cSPS) es un biomarcador de patología computacional que integra la distancia espacial entre células HER2-positivas y HER2-negativas con la intensidad de expresión, generando un score continuo predictivo de respuesta. Estudio ASCO GI 2023 en DESTINY-Gastric01. Pacientes BM+ mPFS 8.3 vs 3.9 meses.[16]
- Cáncer de mama: Ma et al. (2025) en ensayo FASCINATE-N. En HR-positivo, la agregación espacial de células HER2 3+ se asocia con menor respuesta. Notablemente, en tumores HR-negativos, el predictor principal de respuesta fue la infiltración inmune en lugar de la agregación HER2, lo que refuerza la complejidad del microambiente tumoral reconocida como limitación del modelo.[17]
PILAR 5: La Discordancia HER2 Entre Biopsia Primaria y Metástasis
El modelo incluye un ajuste por riesgo preanalítico respaldado por el estudio HEROIC (2025, n=3.546):
En el estudio HEROIC (ASCO 2025, n=3.546), la discordancia HER2 entre primario y metástasis fue del 20.2% en la era HER2-ultralow. Entre los pacientes tratados con T-DXd (n=1.052), la ORR fue del 55.7% cuando ambas muestras expresaban HER2 (cohorte 1), del 53.1% cuando solo la metástasis expresaba HER2 (cohorte 3), pero solo del 13.0% cuando la metástasis era HER2-null (cohorte 2). Esto demuestra que el HER2 de la metástasis predice mejor la respuesta al T-DXd que el del tumor primario.[18]
PILAR 6: Modelos Farmacocinéticos Validan la Difusión Espacial
- Burton et al. (2019): Modelo QSP que demuestra que la exposición de células distantes depende fuertemente de la proximidad espacial.[19]
- Vasalou et al. (2015): Modelo de penetración y transporte intersticial.[20]
- Wei et al. (2024): Cuantificación espaciotemporal de la actividad bystander y demostración de la mejora de la penetración en tumores sólidos (más allá de detallar la Binding Site Barrier).[21]
Resumen de la Validación Clínica
| Componente del Modelo | Evidencia de Validación | Referencias |
|---|---|---|
| Eficacia T-DXd en HER2-positivo | DESTINY-Breast01/03: ORR 60.9-79%, PFS 19.4-29.0 meses | [1,2] |
| Eficacia T-DXd en HER2-low | DESTINY-Breast04: PFS 9.9 vs 5.1 meses | [3,4] |
| Eficacia T-DXd en HER2-ultralow | DESTINY-Breast06: ORR 57.3% (ITT); 61.8% en subgrupo ultralow | [5] |
| Efecto bystander visualizado | Suzuki 2021: DXd difunde a áreas HER2-negativas | [8] |
| Penetración payload 30-80 μm | Khera 2021/2022: Mapeo farmacodinámico celular | [9,10] |
| Heterogeneidad predice resistencia | Hu 2026: pCR 24.5% (HQE alto) vs 62.5% (bajo) | [13] |
| Proximidad espacial predice respuesta | cSPS (ASCO GI 2023): mPFS 8.3 vs 3.9 meses | [16] |
| Discordancia HER2 afecta respuesta | HEROIC 2025: ORR 55.7% vs 13.0% | [18] |
| Modelos QSP validan difusión | Burton 2019, Vasalou 2015: Gradientes espaciales | [19,20] |
Referencias Bibliográficas
- Saura C, Modi S, Krop I, et al. Trastuzumab Deruxtecan in Previously Treated Patients With HER2-positive Metastatic Breast Cancer: Updated Survival Results From a Phase II Trial (DESTINY-Breast01). Ann Oncol. 2024;35(3):302-307.[1b]Modi S, et al. Trastuzumab Deruxtecan in Previously Treated HER2-Positive Breast Cancer (análisis primario). N Engl J Med. 2020;382(7):610-621.
- Cortés J, et al. Trastuzumab Deruxtecan versus Trastuzumab Emtansine for Breast Cancer. NEJM. 2022.
- Modi S, et al. Trastuzumab Deruxtecan in Previously Treated HER2-Low Advanced Breast Cancer. NEJM. 2022.
- Modi S, et al. Trastuzumab Deruxtecan in HER2-low MBC: Long-Term Survival DESTINY-Breast04. Nature Med. 2025.
- Bardia A, et al. Trastuzumab Deruxtecan after Endocrine Therapy in Metastatic Breast Cancer. NEJM. 2024.
- Dilawari A, et al. FDA Approval Summary: T-DXd for HR+, HER2-Low or HER2-Ultralow Breast Cancer. JCO. 2025.
- Narayan P, et al. FDA Approval Summary: Fam-Trastuzumab Deruxtecan-nxki for HER2-Low MBC. JCO. 2023.
- Suzuki M, et al. Visualization of Intratumor PK of T-DXd in HER2 Heterogeneous Model Using PID. Clin Cancer Res. 2021.
- Khera E, et al. Quantifying ADC Bystander Payload Penetration With Cellular Resolution. Neoplasia. 2021.
- Khera E, et al. Cellular-Resolution Imaging of Bystander Payload Tissue Penetration. Mol Cancer Ther. 2022.
- Tsao LC, et al. Effective Extracellular Payload Release and Immunomodulatory Interactions Govern T-DXd. Nature Comms. 2025.
- Filho OM, et al. Impact of HER2 Heterogeneity on Treatment Response: Phase II Neoadjuvant T-DM1 + Pertuzumab. Cancer Discov. 2021.
- Hu J, et al. Predictors of Response to Neoadjuvant Therapy in HER2-Positive Breast Cancer and HQE. Mod Pathol. 2026.
- Li Z, et al. HER2 Heterogeneity and Treatment Response-Associated Profiles in HER2-positive Breast Cancer. JCI. 2024.
- Goyette MA, et al. HER2 Heterogeneous Breast Cancer Models Reveal Novel Therapeutic Targets. Cancer Discov. 2026.
- Kapil A, et al. Computational pathology–based HER2 quantification to identify novel biomarkers in gastric cancer. J Clin Oncol. 2023;41(suppl 4; abstr 449).
- Ma D, et al. Spatial Determinants of Antibody-Drug Conjugate SHR-A1811 Efficacy in Neoadjuvant Treatment. Cancer Cell. 2025.
- Zou Y, et al. Impact of HER2-ultralow heterogeneity and optimal threshold on T-DXd efficacy (HEROIC). J Clin Oncol 43, 2025, suppl 16; abstr 1117.
- Burton JK, et al. A Systems Pharmacology Model for Drug Delivery to Solid Tumors by ADCs. AAPS Journal. 2019.
- Vasalou C, et al. A Mechanistic Tumor Penetration Model to Guide Antibody Drug Conjugate Design. PLoS One. 2015.
- Wei Q, et al. Spatiotemporal Quantification of HER2-targeting Antibody-Drug Conjugate Bystander Activity. Clin Cancer Res. 2024.